Исследование Virlaza относительно воспаления и фиброза легких при COVID-19
РУКОВОДИТЕЛЬ ИССЛЕДОВАНИЯ:
ПРОФЕССОР Д-Р РОДОЛЬФО ДЕ ПАУЛА ВИЕЙРА (RODOLFO DE PAULA VIEIRA)
МЕСТО ИССЛЕДОВАНИЯ: Лаборатория легочной иммунологии и иммунологии физических упражнений Федерального университета Сан-Паулу (UNIFESP), Rua Talim 330, кабинет 119, Сан-Жозе-дус-Кампус, Бразилия, 12231-280.
Эксперименты проводились с использованием двух видов клеток, играющих основную роль в патофизиологии COVID-19 — BEAS-2B (бронхиальные эпителиальные клетки) и MRC-5 (клетки фибробластов легких), стимуляция которых проводилась с помощью клеток цельной крови пациента с вирусной нагрузкой COVID-19 в диапазоне 15–18 пороговых циклов (CT), полученных в острой фазе заболевания (не позднее 24 часов после госпитализации).
Таким образом, в 2 мл свежей цельной крови пациента с COVID-19 культивировали 5x104 клеток линии BEAS-2B и 1x104 клеток линии MRC-5 для начальной инкубации с 50 мкл VIRLAZA (Immune Cov) в течение 1 часа с последующим дополнительным периодом инкубации 3 часа в СО2-инкубаторе при 5 % СО2 и 37 °С. После 4 часов инкубации клетки собирали и центрифугировали при 900 g и 4° в течение 7 минут. Надосадочную жидкость использовали для определения содержания провоспалительных цитокинов (IL-1β, IL-6, IL-8 и TNF-α), которые являются ключевыми для патофизиологии COVID-19, прогрессирования и тяжести заболевания, а также противовоспалительных цитокинов (IL-1RA и IL-10). Результаты показали, что VIRLAZA (Immune Cov) в значительной степени ингибирует активацию клеток бронхиального эпителия (BEAS-2B), как это происходит в естественных условиях in vivo при заболевании COVID-19, поскольку VIRLAZA (Immune Cov) ингибирует синтез и высвобождение IL-1β (р < 0,001), IL-6 (р < 0,05), IL-8 (р < 0,05) и TNF-α (р < 0,001).
Следует отметить, что согласно применяемому протоколу добавление VIRLAZA (Immune Cov) только после 1-часовой инкубации клеток BEAS-2B с инфицированной кровью пациента с COVID-19 убедительно свидетельствует о том, что VIRLAZA (Immune Cov) можно успешно использовать на ранней стадии заболевания у пациентов с COVID-19 для предотвращения его обострения, которое происходит из-за интенсивного синтеза и высвобождения провоспалительных цитокинов клетками бронхиального эпителия.
Что касается возможного иммунологического механизма, лежащего в основе таких эффектов, настоящее исследование показало, что VIRLAZA (Immune Cov) индуцирует синтез и высвобождение IL-1RA в клетках BEAS-2B, который является мощным эндогенным противовоспалительным цитокином. Кроме того, после такой первоначальной провоспалительной реакции у пациентов с COVID-19 наблюдается активация фибробластов легких, что приводит к развитию фиброза легких, ухудшению функции легких, качества жизни и общего состояние здоровья таких пациентов в течение длительного периода времени.
В данном случае настоящее исследование показало, что VIRLAZA (Immune Cov) эффективно снижает активацию фибробластов легких (клетки MRC-5) за счет снижения синтеза и высвобождения IL-1β (p < 0,001), IL-6 (p < 0,001) и TNF-α (p < 0,001), являющихся классическими цитокинами, используемыми в качестве биомаркеров активации фибробластов.
Важно отметить, что уровни IL-8 не изменялись в клетках линии MRC-5 после стимуляции инфицированной кровью пациентов с COVID-19, а также не изменялись после стимуляции с помощью VIRLAZA (Immune Cov). В этом случае гипотеза о том, что VIRLAZA (Immune Cov) также может ингибировать фиброз легких, наблюдаемый в большинстве тяжелых случаев COVID-19, является внушающей доверие.
К тому же, что касается возможного противовоспалительного иммунологического механизма, принимающего участие в оказываемых VIRLAZA (Immune Cov) эффектах, то он может индуцировать синтез и высвобождение противовоспалительного цитокина IL-1RA, являющегося триггерным противовоспалительным цитокином, предполагающим дезактивацию фибробластов легких, индуцированную COVID-19.
Таким образом, с учетом этих взаимно не противоречивых результатов мы можем доказать мощный противовоспалительный эффект VIRLAZA (Immune Cov) применительно COVID-19, открыть новые возможности для вмешательства на ранней стадии у людей с COVID-19. Следовательно, принимая во внимание такие результаты, срочно требуется проведение клинического исследования с использованием VIRLAZA (Immune Cov) у пациентов с COVID-19 различной степени тяжести.
Ниже представлены графики, на которых отображены все результаты.
*** p < 0,001; ** p < 0,01 и * p < 0,05. Co — контрольная группа (только клетки);
IC — группа VIRLAZA (ImmuneCov) (клетки + VIRLAZA (ImmuneCov);
SarsCov2 — группа с наличием инфекции (клетки, инкубированные с кровью пациента, инфицированного COVID-19) и
SarsCov2 + IC — группа с наличием инфекции, обработанная VIRLAZA (Immune Cov). Следует уточнить, что также измерялись уровни IL-10 (иммуномодулирующего, а иногда и противовоспалительного цитокина), но различий между всеми группами обнаружено не было.
ПРОФЕССОР Д-Р РОДОЛЬФО ДЕ ПАУЛА ВИЕЙРА (RODOLFO DE PAULA VIEIRA)
МЕСТО ИССЛЕДОВАНИЯ: Лаборатория легочной иммунологии и иммунологии физических упражнений Федерального университета Сан-Паулу (UNIFESP), Rua Talim 330, кабинет 119, Сан-Жозе-дус-Кампус, Бразилия, 12231-280.
Эксперименты проводились с использованием двух видов клеток, играющих основную роль в патофизиологии COVID-19 — BEAS-2B (бронхиальные эпителиальные клетки) и MRC-5 (клетки фибробластов легких), стимуляция которых проводилась с помощью клеток цельной крови пациента с вирусной нагрузкой COVID-19 в диапазоне 15–18 пороговых циклов (CT), полученных в острой фазе заболевания (не позднее 24 часов после госпитализации).
Таким образом, в 2 мл свежей цельной крови пациента с COVID-19 культивировали 5x104 клеток линии BEAS-2B и 1x104 клеток линии MRC-5 для начальной инкубации с 50 мкл VIRLAZA (Immune Cov) в течение 1 часа с последующим дополнительным периодом инкубации 3 часа в СО2-инкубаторе при 5 % СО2 и 37 °С. После 4 часов инкубации клетки собирали и центрифугировали при 900 g и 4° в течение 7 минут. Надосадочную жидкость использовали для определения содержания провоспалительных цитокинов (IL-1β, IL-6, IL-8 и TNF-α), которые являются ключевыми для патофизиологии COVID-19, прогрессирования и тяжести заболевания, а также противовоспалительных цитокинов (IL-1RA и IL-10). Результаты показали, что VIRLAZA (Immune Cov) в значительной степени ингибирует активацию клеток бронхиального эпителия (BEAS-2B), как это происходит в естественных условиях in vivo при заболевании COVID-19, поскольку VIRLAZA (Immune Cov) ингибирует синтез и высвобождение IL-1β (р < 0,001), IL-6 (р < 0,05), IL-8 (р < 0,05) и TNF-α (р < 0,001).
Следует отметить, что согласно применяемому протоколу добавление VIRLAZA (Immune Cov) только после 1-часовой инкубации клеток BEAS-2B с инфицированной кровью пациента с COVID-19 убедительно свидетельствует о том, что VIRLAZA (Immune Cov) можно успешно использовать на ранней стадии заболевания у пациентов с COVID-19 для предотвращения его обострения, которое происходит из-за интенсивного синтеза и высвобождения провоспалительных цитокинов клетками бронхиального эпителия.
Что касается возможного иммунологического механизма, лежащего в основе таких эффектов, настоящее исследование показало, что VIRLAZA (Immune Cov) индуцирует синтез и высвобождение IL-1RA в клетках BEAS-2B, который является мощным эндогенным противовоспалительным цитокином. Кроме того, после такой первоначальной провоспалительной реакции у пациентов с COVID-19 наблюдается активация фибробластов легких, что приводит к развитию фиброза легких, ухудшению функции легких, качества жизни и общего состояние здоровья таких пациентов в течение длительного периода времени.
В данном случае настоящее исследование показало, что VIRLAZA (Immune Cov) эффективно снижает активацию фибробластов легких (клетки MRC-5) за счет снижения синтеза и высвобождения IL-1β (p < 0,001), IL-6 (p < 0,001) и TNF-α (p < 0,001), являющихся классическими цитокинами, используемыми в качестве биомаркеров активации фибробластов.
Важно отметить, что уровни IL-8 не изменялись в клетках линии MRC-5 после стимуляции инфицированной кровью пациентов с COVID-19, а также не изменялись после стимуляции с помощью VIRLAZA (Immune Cov). В этом случае гипотеза о том, что VIRLAZA (Immune Cov) также может ингибировать фиброз легких, наблюдаемый в большинстве тяжелых случаев COVID-19, является внушающей доверие.
К тому же, что касается возможного противовоспалительного иммунологического механизма, принимающего участие в оказываемых VIRLAZA (Immune Cov) эффектах, то он может индуцировать синтез и высвобождение противовоспалительного цитокина IL-1RA, являющегося триггерным противовоспалительным цитокином, предполагающим дезактивацию фибробластов легких, индуцированную COVID-19.
Таким образом, с учетом этих взаимно не противоречивых результатов мы можем доказать мощный противовоспалительный эффект VIRLAZA (Immune Cov) применительно COVID-19, открыть новые возможности для вмешательства на ранней стадии у людей с COVID-19. Следовательно, принимая во внимание такие результаты, срочно требуется проведение клинического исследования с использованием VIRLAZA (Immune Cov) у пациентов с COVID-19 различной степени тяжести.
Ниже представлены графики, на которых отображены все результаты.
*** p < 0,001; ** p < 0,01 и * p < 0,05. Co — контрольная группа (только клетки);
IC — группа VIRLAZA (ImmuneCov) (клетки + VIRLAZA (ImmuneCov);
SarsCov2 — группа с наличием инфекции (клетки, инкубированные с кровью пациента, инфицированного COVID-19) и
SarsCov2 + IC — группа с наличием инфекции, обработанная VIRLAZA (Immune Cov). Следует уточнить, что также измерялись уровни IL-10 (иммуномодулирующего, а иногда и противовоспалительного цитокина), но различий между всеми группами обнаружено не было.

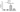
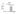
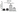

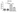





Разработка и исследования компании "LibiPharm" - "ЛибиФарм" Израиль.
© 2024 Calpton SIA. Все права защищены.
Мы принимаем




